15个大品种,进口仿制药来了(附名单)
加入日期:2019/5/14 9:04:17 查看人数: 1694 作者:admin
近日,诺华宣布旗下山德士的子公司Lek Pharmaceuticals d.d.生产的瑞舒伐他汀通过了一致性评价,成为首个外资药企过评的仿制药。此次Lek的瑞舒伐他汀钙片通过一致性评价,证实了进口仿制药在中国也需要过评。中国仿制药市场潜力巨大,外资药企怎会舍得拱手相让。数据显示,除了瑞舒伐他汀外,目前还有14个进口仿制药申报一致性评价。
首个通过一致性评价的进口仿制药
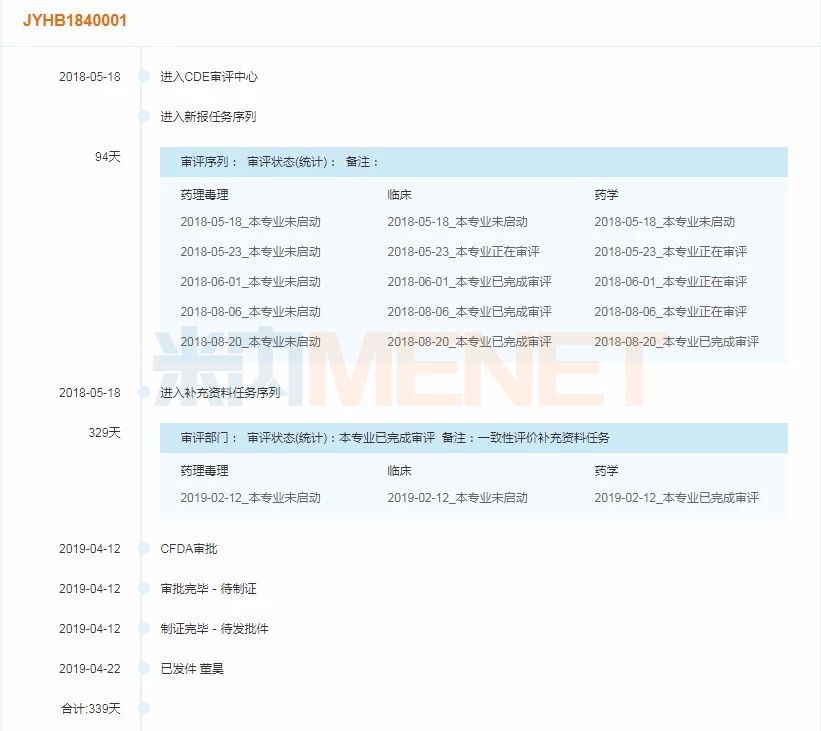
图1:Lek Pharmaceuticals d.d. 瑞舒伐他汀钙片(受理号JYHB1840001)审评时间轴
(米内网MED药品审评数据库2.0)
据米内网数据显示,Lek Pharmaceuticals d.d. 的瑞舒伐他汀钙片受理号JYHB1840001、JYHB1840002均在2018年5月18日获得承办,2019年4月获批通过一致性评价,用时在330天左右。
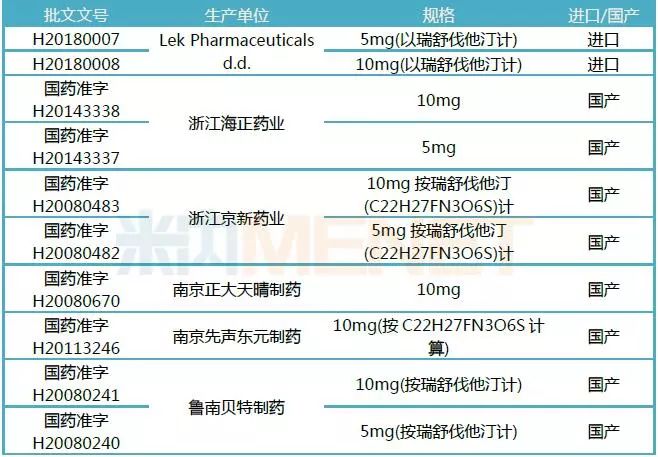
表1:目前通过一致性评价的瑞舒伐他汀钙片
(米内网一键检索)
截至2019年5月9日,瑞舒伐他汀钙片通过或视同通过一致性评价的企业有6家,该产品在2017年中国公立医疗机构(中国城市公立医院、县级公立医院、城市社区中心及乡镇卫生院)终端销售额达到50.2亿元。在去年年底的“4+7带量采购”中,瑞舒伐他汀钙片为入围品种,浙江京新药业以21.8元/盒(10mg*28片)中标。
京新药业在2018年年报中提到,为保证4+7集采产品的保质保量供货,公司内部将通过生产线产品的合理调配、生产批次的放大验证、现场管理的精细化等管理措施,提升制剂产能,保证市场供给。带量采购已成为接下来医药界的主旋律,通过一致性评价的仿制药将成为争夺市场的主力。
15个进口仿制药申报一致性评价,13个仍在审
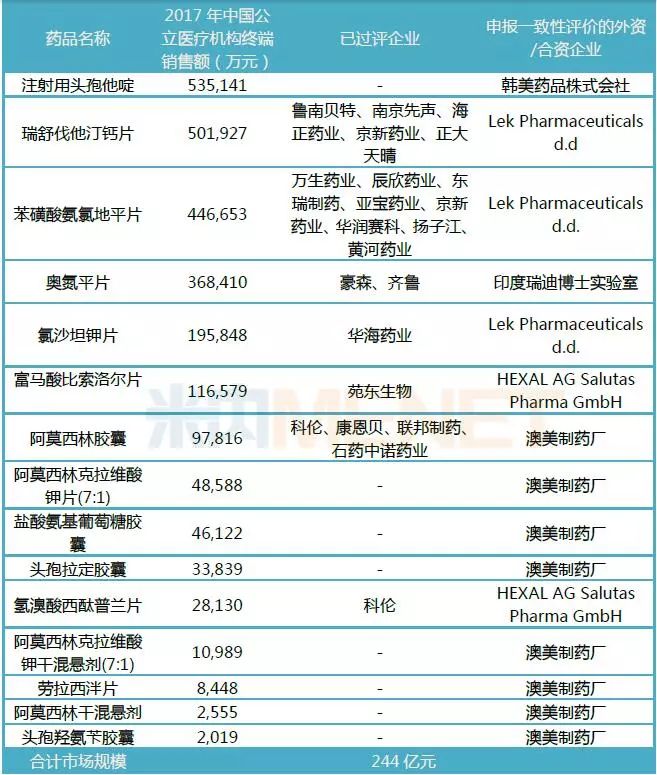
表2:目前申报一致性评价的15个进口仿制药相关情况
(米内网数据库)
据米内网MED中国药品审评数据库2.0数据显示,截至目前,共有15个进口仿制药申报一致性评价,其中Lek Pharmaceuticals d.d的瑞舒伐他汀钙片已经过评,HEXAL AG Salutas Pharma GmbH(诺华旗下公司)的氢溴酸西酞普兰片(受理号JYHB1850001)已发件,推测尚未通过一致性评价,其余13个进口仿制药的一致性评价补充申请均在审评审批中。
这15个进口仿制药不乏10亿以上大品种,目前除了瑞舒伐他汀钙片、苯磺酸氨氯地平片、奥氮平片、氯沙坦钾片、富马酸比索洛尔片已有过评企业外,注射用头孢他啶目前申报一致性评价的国内企业仅有齐鲁制药,最终是国内企业更胜一筹还是韩美药品株式会社突围成功,我们静待结果,但目前注射剂一致性评价的进度较慢,估计还需等待一段较长的时间才能有定论。
图2:注射用头孢他啶一致性评价补充申请情况
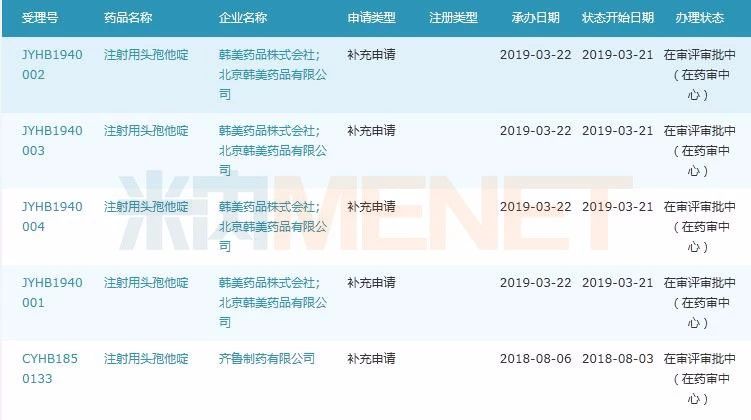
(米内网MED药品审评数据库2.0)
此外,上述过亿规模的产品中,阿莫西林克拉维酸钾片(7:1)、盐酸氨基葡萄糖胶囊、头孢拉定胶囊以及阿莫西林克拉维酸钾干混悬剂(7:1)暂无企业通过一致性评价。
目前市场上的阿莫西林克拉维酸钾片(7:1)有两家企业生产,该产品申报一致性评价的企业目前仅有澳美制药厂;市场上的阿莫西林克拉维酸钾干混悬剂(7:1)仅有澳美制药厂生产,同时该公司也申报了一致性评价。
图3:盐酸氨基葡萄糖胶囊一致性评价补充申请情况

(米内网MED药品审评数据库2.0)
盐酸氨基葡萄糖胶囊为抗炎药和抗风湿药,2017年在中国公立医疗机构终端的销售额为4.6亿元,澳美制药厂超过51%、北京康必得药业占20%、浙江诚意药业占20%、北京葡立药业8%左右。目前除了澳美制药厂外,浙江诚意药业以及北京葡立药业均有申报一致性评价,涉及的受理号均在审评审批中。
图4:头孢拉定胶囊一致性评价补充申请情况
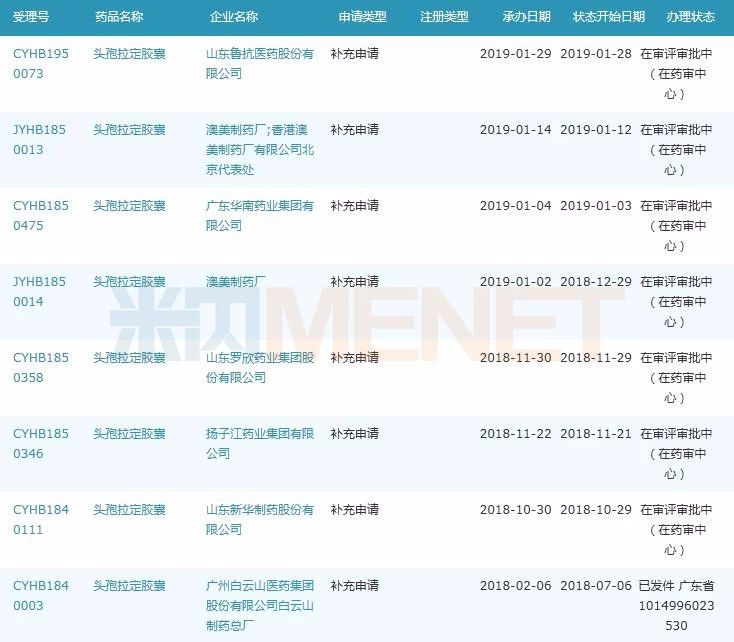
(米内网MED药品审评数据库2.0)
头孢拉定胶囊为全身用抗细菌药,2017年在中国公立医疗机构终端的销售额为3.38亿元,从市场份额来看,湖南科伦制药占比超过20%、扬子江药业集团、山东罗欣药业集团、山东鲁抗医药、施贵宝占比均超10%。目前除了澳美制药厂外,山东鲁抗医药、广东华南药业集团、山东罗欣药业集团、扬子江药业集团、山东新华制药的一致性评价补充申请均在审评审批中,广州白云山医药集团的受理号已发件,CDE审评建议为不批准。
这个进口仿制药视同通过一致性评价
图5:注射用头孢唑林钠/氯化钠注射液的审批情况

(米内网MED药品审评数据库2.0)
图6:注射用头孢唑林钠/氯化钠注射液审评时间轴
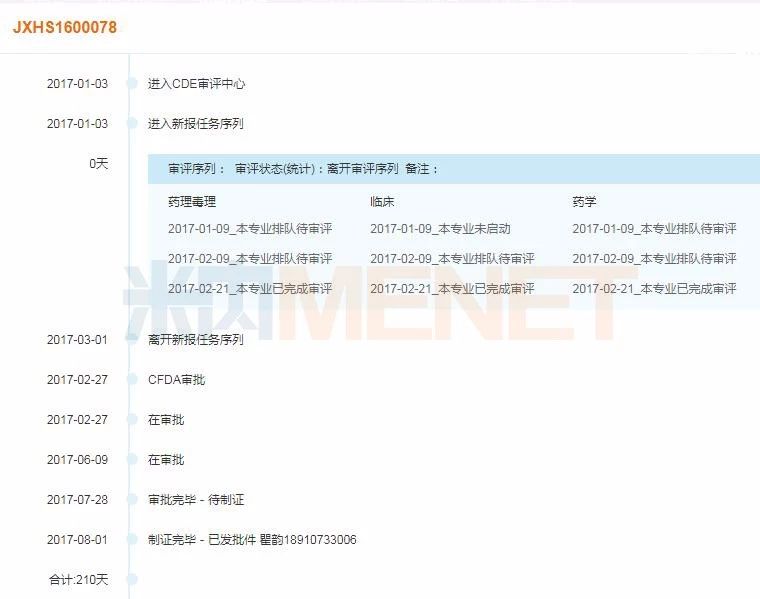
(米内网MED药品审评数据库2.0)
注射用头孢唑林钠/氯化钠注射液为全身用抗细菌药,大冢制药按照5.2类注册的进口仿制药申报,2017年7月26日被纳入中国上市药品目录集,收录类别为按化学药品新注册分类批准的仿制药,视同通过一致性评价。
表3:目前通过或视同通过一致性评价的注射剂
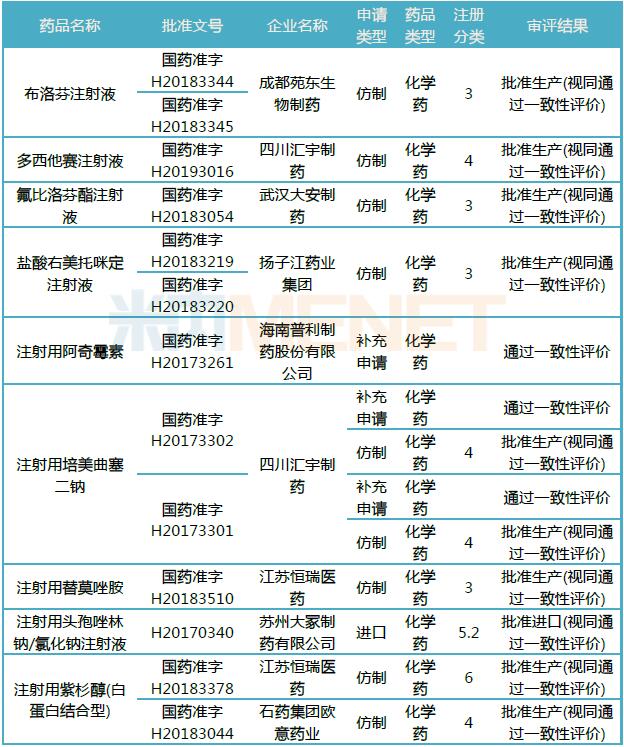
(米内网MED药品审评数据库2.0)
注射剂一致性评价工作进度缓慢,据米内网数据显示,目前通过或视同通过一致性评价的注射剂有9个,其中8个是按化学药品新注册分类批准的仿制药(注射用培美曲塞二钠的4类仿制以及补充申请均获批),可见国家层面对于注射剂的审评、监管力度也在逐渐加大。
结语
目前国内仿制药的一致性评价工作越趋激烈,随着带量采购的进一步推进,中标企业也陆续获得了实惠,行业内外对一致性评价的支持力度也逐渐加大。在我们紧盯着国内仿制药如何挑战原研,争夺市场的同时,外资/合资药企的进口仿制药也在蠢蠢欲动,可见未来中国仿制药市场的竞争将更加激烈,高质量的仿制药也将逐渐成为市场主力,推动着我国医药产业向前发展。4+7带量采购文件中提到,原研药、参比制剂、通过或视同通过一致性评价的产品均有资格申报,预计这将成为后续集采品种申报企业的入场券,随着进口仿制药也参与到一致性评价中,后续的集采品种又将迎接着怎样的挑战?我们拭目以待。