上半年进入创新/优先审批通道产品汇总(附名单)
加入日期:2022/7/6 8:58:44 查看人数: 2484 作者:admin
近年来,医疗器械审评审批制度不断深入改革,为保障医疗器械的安全、有效,鼓励医疗器械的研究与创新,国家药监局于2018年11月2日发布了新修订的《创新医疗器械特别审查程序》,这对医疗器械产业创新发展起到了积极作用。同时,为了保障医疗器械临床使用需求,原国家食品药品监督管理总局2016年10月26日发布了《医疗器械优先审批程序》,这为提升人民群众实现更好的卫生健康水平发挥了巨大作用。
总体情况
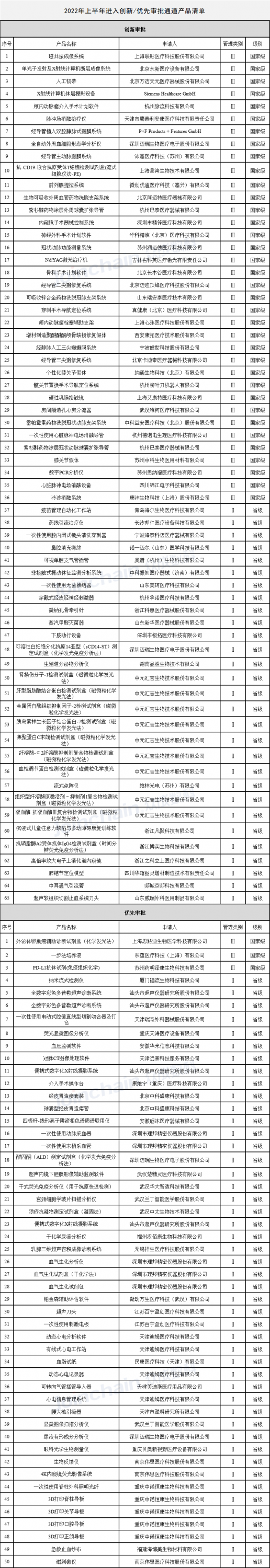
据众成数科(JOINCHAIN)统计,2022年上半年,共计55家企业的65件产品进入创新医疗器械特别审批通道,其中36件产品进入国家级创新审批通道,29件产品进入省级创新审批通道;共计30家企业的50件产品进入优先审批通道,其中3件产品进入国家级优先审批通道,47件产品进入省级优先审批通道。(产品清单见附表1)
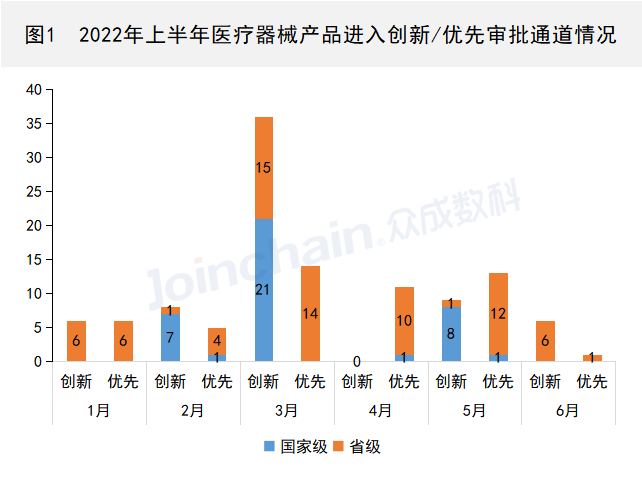
数据来源:JOINCHAIN®众成数科
区域分布
1、 创新审批
从区域分布来看,2022年上半年进入创新审批通道的产品中,63件为国产产品,2件为进口产品。其中产品数量位列前三的省市分别为浙江省(14件)、北京市(10件)和重庆市(9件)。
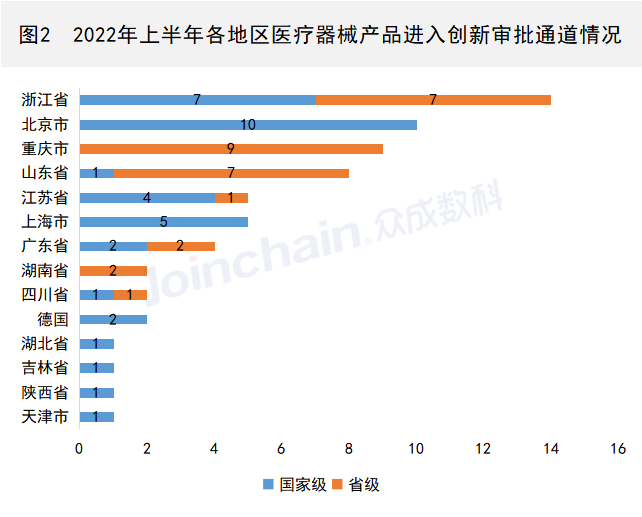
数据来源:JOINCHAIN®众成数科
2、优先审批
2022年上半年进入优先审批通道产品数量位列前三的省市分别为广东省(11件)、天津市(9件)和重庆市(8件)。
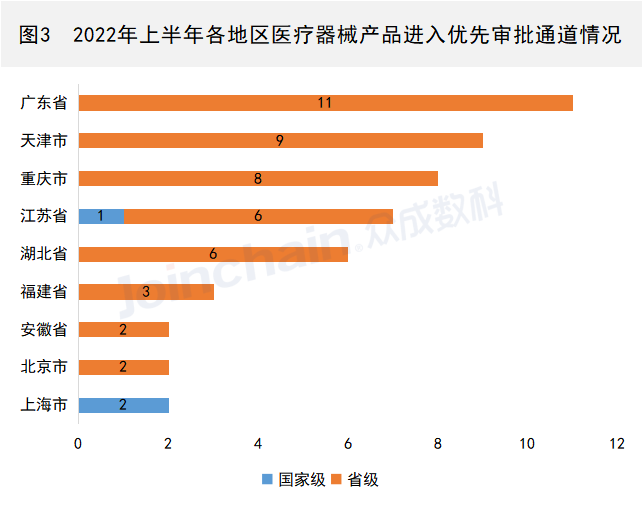
数据来源:JOINCHAIN®众成数科
产品类型
1、创新审批
从产品类型来看,无源植入器械共有14件Ⅲ类产品进入创新审批通道,体外诊断试剂分别有11件Ⅱ类产品和1件Ⅲ类产品进入创新审批通道,有源手术器械分别有1件Ⅱ类产品和8件Ⅲ类产品进入创新审批通道。
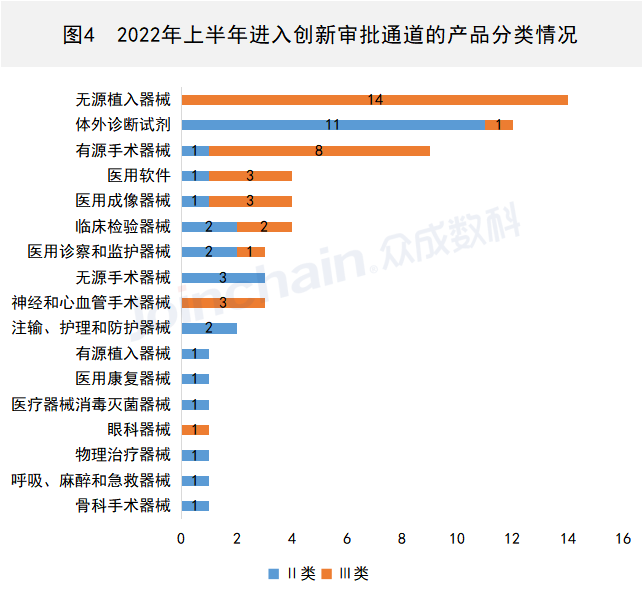
数据来源:JOINCHAIN®众成数科
2、优先审批
进入优先审批通道的产品中,产品数量前三的产品类别分别是体外诊断试剂(9件)、临床检验器械(8件)和医用成像器械(6件),其中仅有体外诊断试剂类含有Ⅲ类产品,数量为3件。
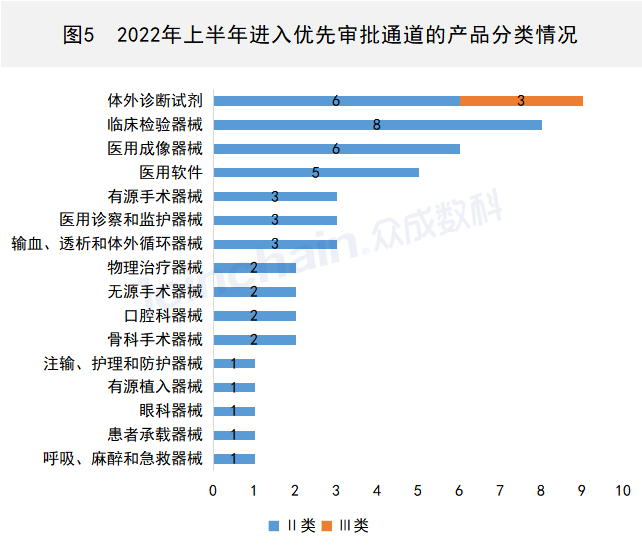
数据来源:JOINCHAIN®众成数科
(附表1)